Contente
Outras SeçõesO hidrogênio é o elemento mais leve e tem muitos usos industriais, incluindo a criação de gorduras hidrogenadas para uso na cozinha e a produção de hidrocarbonetos a partir do carvão. É uma parte essencial das moléculas de água e pode ser separada com uma pequena quantidade de eletricidade. Você também pode produzir gás hidrogênio usando alguns metais ativos e ácidos fortes. Ambos os métodos são relativamente simples e permitem coletar gás hidrogênio.
Passos
Método 1 de 2: usando deslocamento de água com metais ativos
Reúna os materiais necessários. Para coletar hidrogênio usando a reação de mistura de um ácido forte com um metal ativo, você precisará de: um Erlenmeyer, uma rolha de borracha, tubo de plástico, água destilada, tubos de ensaio, um grande recipiente, ácido clorídrico 3 molar (HCl) e pelotas de magnésio ou zinco.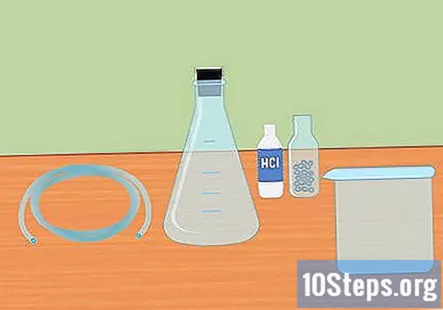
- Um Erlenmeyer é um frasco de vidro de fundo cônico e gargalo cilíndrico.
- A rolha de borracha é para o topo do frasco e precisa ter um orifício no meio para a passagem do tubo.
- Magnésio ou zinco funcionarão para esta experiência, você não precisa de ambos.
- Alguns desses suprimentos podem precisar ser comprados online ou em uma loja de suprimentos de laboratório.

Use equipamento de proteção adequado. Ao trabalhar com um ácido forte como o ácido clorídrico, certifique-se de tomar as devidas precauções de segurança. O uso de jaleco, luvas, sapatos fechados e proteção para os olhos são essenciais.- Os óculos devem envolver os lados dos olhos para protegê-los de respingos.
- Use luvas adequadas para manter uma boa destreza das mãos e dos dedos.
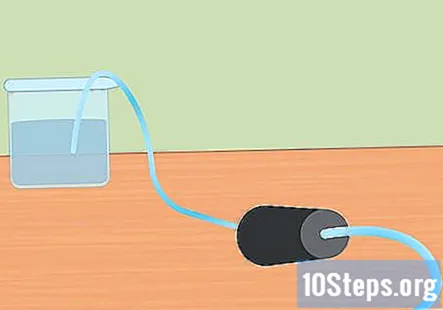
Prepare a configuração experimental. Insira uma extremidade do tubo no orifício da rolha de borracha. Você deseja que o tubo atravesse a tampa de borracha e fique ligeiramente saliente na extremidade. Encha o recipiente grande com água e coloque a extremidade livre do tubo na água. Quando o experimento começar, você colocará a rolha de borracha no frasco Erlenmeyer.- Deixe essas peças de lado até que esteja pronto para usá-las.
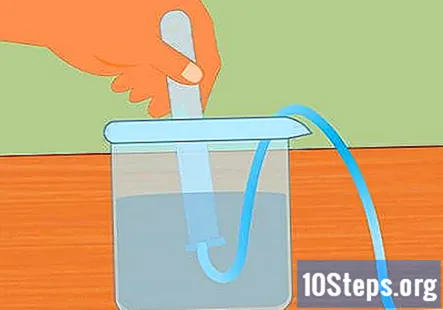
Mergulhe o tubo de ensaio na água. Pegue pelo menos um tubo de ensaio (você pode usar mais se quiser coletar mais hidrogênio) e mergulhe-o na água. Incline o tubo para que todas as bolhas de ar possam escapar. Coloque o tubo em cima do tubo submerso preso à rolha de borracha na extremidade oposta.- É essencial que todas as bolhas de ar sejam removidas do tubo antes de você começar. Se não forem, o gás coletado no tubo será mais do que apenas hidrogênio.
Adicione ácido clorídrico ao frasco Erlenmeyer. Adicione ácido clorídrico suficiente para encher o frasco até a metade. Cerca de 100 mL devem ser suficientes. Certifique-se de que o frasco esteja limpo e seco antes de adicionar o ácido. Use luvas de borracha e tenha cuidado ao encher o frasco.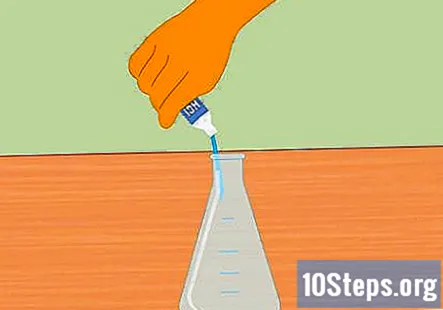
- Tome cuidado para não derramar água no ácido. Água adicionada ao ácido pode causar explosão e ferimentos.
Comece a reação química adicionando grânulos de metal ao HCl. Adicione um punhado de pellets de zinco ou magnésio ao ácido clorídrico do frasco. A quantidade exata que você coloca não é importante, mas um pequeno punhado deve ser suficiente para iniciar a reação.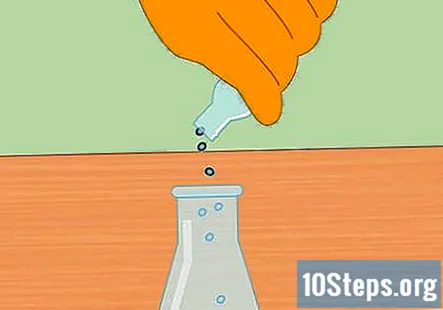
- Após adicionar os pellets, coloque a rolha no frasco de forma que o sistema seja fechado.
Colete o hidrogênio em um tubo de ensaio submerso. Conforme o metal reage com o ácido, o gás hidrogênio é produzido. Este hidrogênio viaja para o topo do frasco, através do tubo e para dentro do tubo de ensaio submerso na água. O gás irá deslocar a água e você deverá ver uma bolha se formar no topo do tubo de ensaio.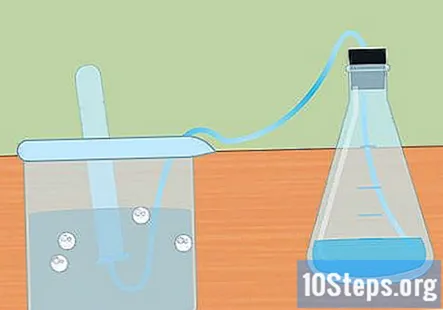
- Quando o tubo de ensaio se encher de hidrogênio, mergulhe outro tubo com água e coloque-o sobre o tubo. Você pode coletar tanto hidrogênio quanto é produzido por sua reação.
- Mantenha os tubos de ensaio voltados para baixo para evitar que o gás hidrogênio escape para o ar.
Confirme se o gás é hidrogênio. Para confirmar que o gás é hidrogênio, você pode fazer o que é chamado de teste de tala. Acenda um fósforo e segure-o embaixo do tubo. Você ouvirá um "estalo" ou som agudo, indicando que o hidrogênio está presente.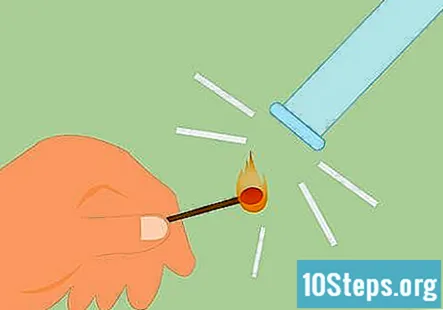
Método 2 de 2: usando eletrólise
Reúna os materiais necessários. Neste experimento, você usará eletricidade para separar os gases de hidrogênio e oxigênio das moléculas de água. Para coletar o gás hidrogênio por meio da eletrólise, você precisará de uma bateria de 9 volts, um lápis, dois tubos de ensaio, um recipiente de plástico, água, bicarbonato de sódio, dois elásticos grandes (opcional) e um clipe de bateria com grampos na extremidade.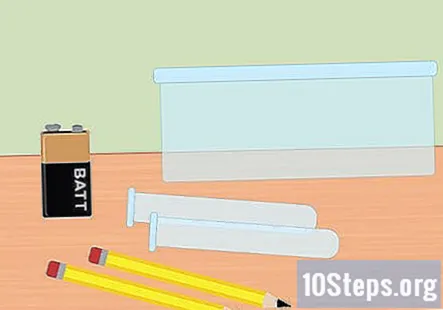
- O lápis deve conter grafite para que funcione. Um lápis número 2 é perfeito. Dois pequenos pedaços de grafite também servirão para isso.
- Um pequeno recipiente ou tigela de armazenamento de alimentos é suficiente.
- Certifique-se de que o clipe da bateria pode caber em uma bateria de 9 volts e que tem um fio vermelho e preto com pinças de crocodilo na extremidade. Esses grampos serão usados para conectar seu sistema à bateria.
Remova a borracha do lápis e parta o lápis ao meio. Você precisa de dois pedaços de grafite, um para o lado positivo da bateria e para o lado negativo da bateria. Afie ambas as pontas de cada pedaço do lápis em uma ponta. Verifique se o grafite está bem exposto.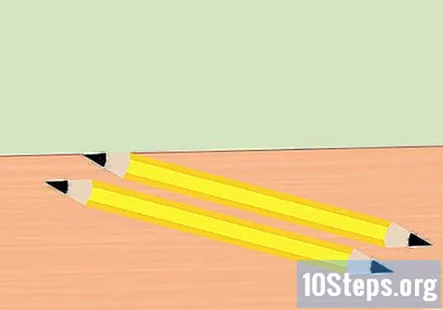
- Esta etapa pode ser ignorada se você já tiver duas peças de grafite puro.
Enrole 2 elásticos ao redor do recipiente em forma de X. Esta etapa é opcional, mas é uma maneira fácil de manter os tubos de ensaio no lugar enquanto o experimento está sendo executado. Estique um elástico sobre o recipiente e estique um segundo elástico sobre ele de modo que cruze sobre o primeiro, formando um X.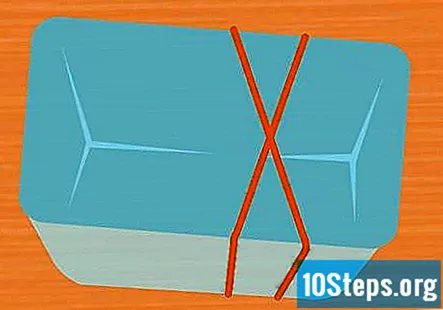
- Se você não usar elásticos, certifique-se de prender os tubos de ensaio com fita ou barbante para que fiquem de cabeça para baixo durante o experimento.
Faça uma solução de bicarbonato de sódio e água. Dissolver o bicarbonato de sódio na água ajudará a conduzir a eletricidade no sistema. A quantidade exata de bicarbonato de sódio adicionado não é importante, mas cerca de 1 colher de chá por 1 xícara de água deve ser suficiente. Mexa até dissolver completamente.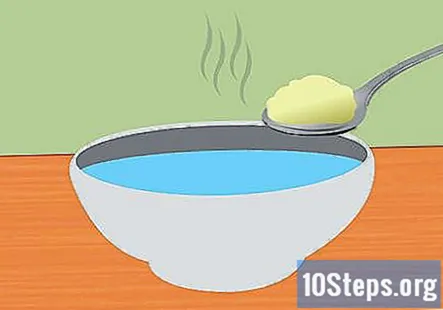
- Use água morna para acelerar a dissolução do bicarbonato de sódio.
Encha o recipiente de plástico e os tubos de ensaio com a solução de bicarbonato de sódio. O recipiente deve ser grande o suficiente para conter os dois tubos de ensaio. Adicione o suficiente da solução para encher o recipiente cerca de três quartos. Mergulhe os tubos de ensaio na solução do recipiente e vire-os de cabeça para baixo. Coloque cada tubo na cruz do elástico X para prendê-lo no lugar.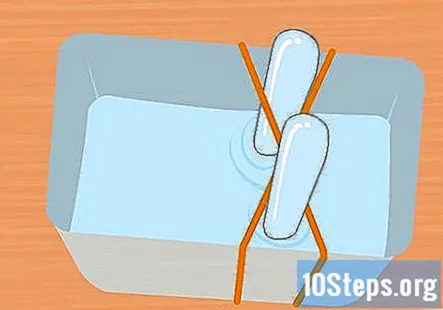
- É muito importante que ambos os tubos de ensaio estejam completamente cheios de água e não permaneçam bolhas de ar.
Prenda as pinças jacaré na grafite. Pegue uma braçadeira do clipe da bateria e prenda-a na ponta de um dos lápis. Certifique-se de que está tocando o máximo possível no grafite. Faça o mesmo com a pinça jacaré restante e o pedaço de lápis.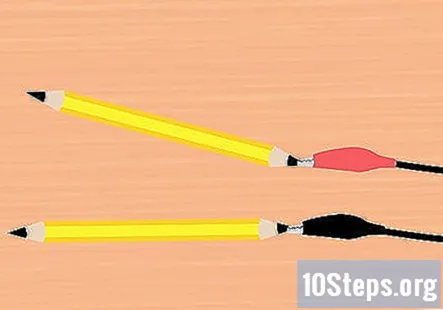
- Um lápis deve ser colocado na pinça vermelha e um lápis na pinça preta.
Deslize a ponta solta do lápis no tubo de ensaio. Mantendo o tubo de ensaio completamente submerso, incline-o levemente para que você possa deslizar a extremidade solta do lápis para dentro do tubo. Repita este processo com o outro lápis e o outro tubo de ensaio.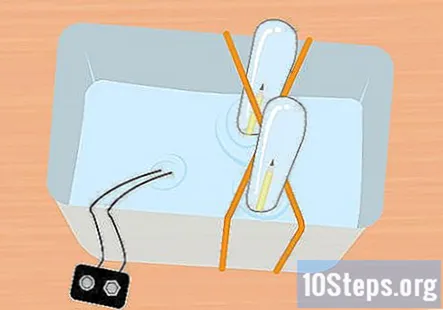
- Nesse ponto, tudo deve estar debaixo d'água e deve haver um lápis dentro de cada tubo de ensaio.
- Mantenha a ponta do clipe da bateria fora da água.
Prenda o clipe da bateria à bateria de 9 volts. Com tudo configurado, você agora está pronto para aplicar a eletricidade fornecida pela bateria de 9 volts. A extremidade do clipe da bateria deve ficar para fora do recipiente, então simplesmente prenda a bateria no lugar. Assim que a bateria for instalada, você deve notar bolhas subindo do final do grafite e flutuando para o topo de cada tubo de ensaio.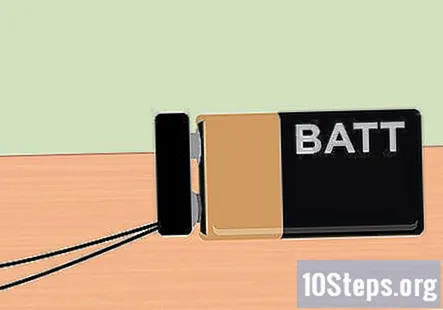
- Se você não vir bolhas produzidas, verifique se as pinças de crocodilo estão firmemente presas ao grafite do lápis. Além disso, verifique se a bateria está totalmente carregada.
- O tubo de ensaio com o fio negativo preso ao lápis estará produzindo hidrogênio, enquanto o tubo de ensaio preso ao fio positivo da bateria estará produzindo oxigênio.
Colete o hidrogênio e o oxigênio nos dois tubos de ensaio até que você tenha alguns centímetros de gás em cada tubo. Lembre-se, o tubo conectado à extremidade negativa da bateria terá o hidrogênio e o oxigênio estará no tubo conectado à extremidade positiva. Remova os tubos de ensaio do frasco, um de cada vez. Mantenha-os de cabeça para baixo e deixe a água escorrer. O gás nos tubos permanecerá, mesmo que você não possa vê-lo.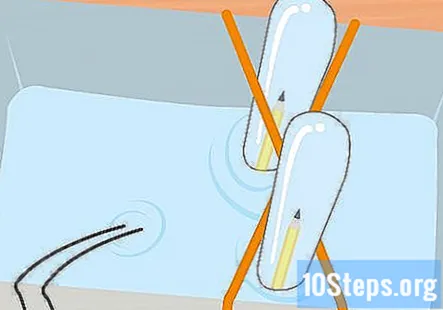
Teste a presença de hidrogênio. Você pode testar a presença de hidrogênio riscando um fósforo e segurando a chama contra o gás. Ele fará um som "pop estridente" muito distinto se for hidrogênio. Você também pode usar uma vela acesa em vez de um fósforo.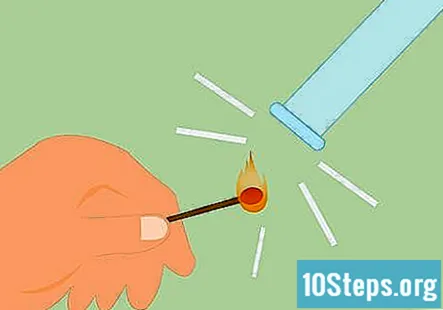
- Para testar o oxigênio no tubo de ensaio que foi conectado ao lado positivo da fonte de energia, apague um fósforo aceso (ou vela) e coloque a extremidade ainda brilhante sob o tubo de ensaio. Se a vela reacender, o oxigênio está presente.
Perguntas e respostas da comunidade
Preciso de dois tubos de ensaio se quiser coletar apenas hidrogênio?

A cientista ambiental Bess Ruff é estudante de doutorado em geografia na Florida State University. Ela recebeu seu mestrado em Ciência e Gestão Ambiental pela Universidade da Califórnia, Santa Bárbara, em 2016. Ela conduziu pesquisas para projetos de planejamento espacial marinho no Caribe e forneceu apoio à pesquisa como bolsista de pós-graduação do Grupo de Pesca Sustentável.

Quanto hidrogênio pode ser coletado com esse experimento simples de eletrólise? E qual seria a pressão do gás hidrogênio?
Depende. A taxa de reação (divisão da água) é baseada na amperagem da bateria e no tempo restante para reagir. Normalmente, o hidrogênio estaria próximo à pressão ao nível do mar, a menos que você faça o experimento em um ambiente muito quente ou frio.
Por que o hidrogênio se acumula no tubo negativo
Devido à forma como as moléculas de água compartilham elétrons, os átomos de hidrogênio são carregados positivamente e os átomos de oxigênio negativamente. Ao extrair os gases, o hidrogênio carregado positivamente será atraído para o tubo negativo, enquanto o oxigênio carregado negativamente será atraído para o tubo positivo.
Por que o gás não escapou do meu tubo coletor de gás?
É o hidrogênio, um gás mais leve que todos os outros, inclusive o hélio, o que significa que ficará no tubo de ensaio enquanto a extremidade fechada do tubo estiver no topo porque os outros gases o deslocam. O motivo pelo qual usamos hélio em vez de hidrogênio é que ele não é inflamável. Isso se deve ao fato de ser um gás nobre (possui uma camada de valência completa de 8 elétrons) e, portanto, não é reativo.
O gás seria muito inflamável?
Sim. Veja o desastre de Hindenburg no YouTube. Os zepelins usavam hidrogênio por ser o gás mais leve e bastante fácil de obter. É também por isso que alguns fabricantes de automóveis estão trabalhando em carros movidos a hidrogênio.
esta é a forma líquida do hidrogênio?
Não - o hidrogênio neste experimento será gasoso
Como faço para liquidificar o hidrogênio? Responda
Avisos
- Cuidado com o hidrogênio puro. É altamente explosivo quando misturado ao ar.
- Certifique-se de que todo o ar restante foi removido do equipamento no qual você está coletando hidrogênio.


